원소의 분류와 주기율
(1) 주기율
① 주기율:원소를 원자 번호 순으로 배열할 때, 성질이 비슷한 원소가 주기적으로 나타나는 것을 주기율이라고 한다.
② 주기율이 나타나는 원인:원소의 화학적 성질을 결정하는 원자가 전자 수가 주기적으로 변하기 때문에 주기율이 나타난다.
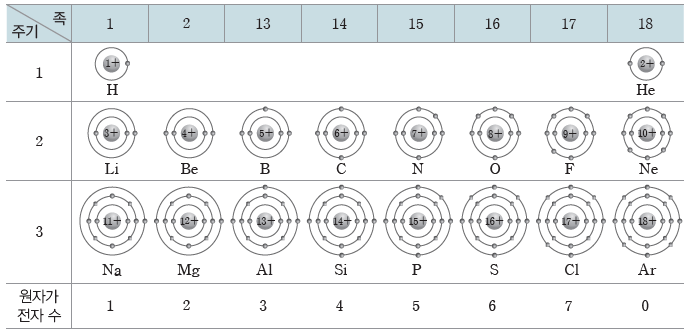
(2) 주기율의 발견 과정
① 라부아지에(1789년):당시에 더 이상 분해할 수 없는 33종의 물질을 기체, 비금속, 금속, 화합물의 네 그룹으로 분류하였다.
② 되베라이너(1816년):화학적 성질이 비슷하고 물리적 성질은 규칙적으로 변하는 세 원소가있다는 것을 알고, 성질이 비슷한 원소를 3개씩 묶어 세 쌍 원소라고 하였다.
③ 뉴랜즈(1865년):원소를 원자량 순으로 나열하면 8번째마다 화학적 성질이 비슷한 원소가나타나는 규칙성을 발견하고, 옥타브설을 발표하였다.
④ 멘델레예프(1869년)
- 당시까지 발견된 63종의 원소를 화학적 성질에 기준을 두어 원자량 순서로 배열하여 주기율표를 만들었는데, 이것이 최초의 주기율표이다.
- 당시까지 발견되지 않은 원소의 자리는 빈칸으로 두고, 주기율표 상의 위치로부터 새로운 원소의 존재 가능성과 성질을 예측하였다.
- 원자량 순서로 배열하였을 때 주기성이 맞지 않는 부분이 있다.
⇨ Ar(원자량 39.9)과 K(원자량 39.1)
⑤ 모즐리(1913년)
- X선 연구를 통해 원소에서 원자핵의 양성자수를 결정하는 방법을 알아내어 원자의 양성자수를 원자 번호로 정하였다.
- 원소의 주기적 성질이 양성자수(원자 번호)와 관련이 있다는 것을 발견하였고, 원소들을 원자 번호 순서대로 배열하여 현재 사용하고 있는 것과 비슷한 주기율표를 완성하였다.
주기율표
(1) 주기율표
원소들을 원자 번호 순으로 배열하여 화학적 성질이 비슷한 원소가 같은 세로줄에 오도록 배열한 표이다.
① 주기
- 주기율표의 가로줄로, 1~7주기가 있다.
- 같은 주기 원소는 바닥상태에서 전자가 들어 있는 전자 껍질 수가 같다. 이때 주기는 전자가 들어 있는 전자 껍질 수와 같다.
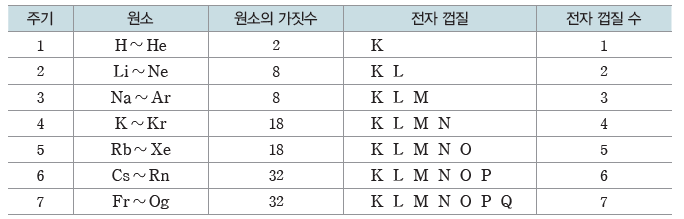
② 족
- 주기율표의 세로줄로, 1~18족이 있다.
- 같은 족 원소는 원자가 전자 수가 같아 화학적 성질이 비슷하다(단, 수소는 1족에 위치하고있지만 비금속 원소로, 1족에 속해 있는 나머지 금속 원소들과는 화학적 성질이 다르다).
- 1~2족, 13~17족의 경우 원자가 전자 수는 족의 끝자리 수와 같다.
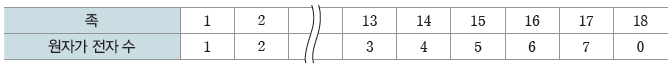
(2) 주기율표에서 원소의 분류
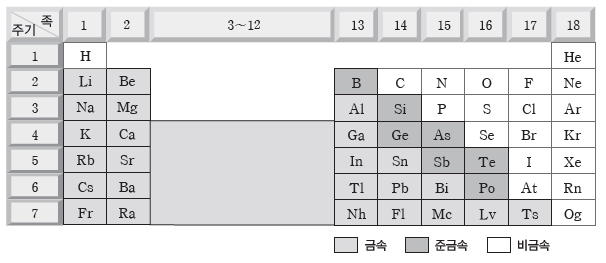
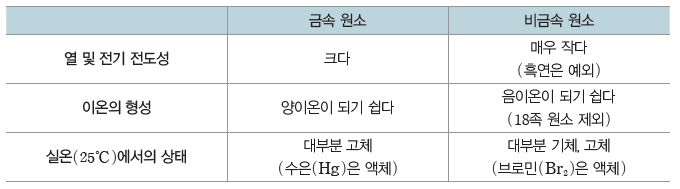
※ 1 atm, 25℃에서의 상태:H, N, O, F, Cl 및 18족 원소는 기체이며, Br, Hg은 액체이고, 나머지는 고체로 존재한다.
① 금속 원소
- 전자를 잃고 양이온이 되기 쉽다. M → Mn++ne–
- 열전도성, 전기 전도성이 크다.
② 비금속 원소 개념 체크
- 전자를 얻어 음이온이 되기 쉽다(18족 원소 제외). X+ne– → Xn-
- 열전도성, 전기 전도성이 매우 작다(탄소(흑연)는 예외).
③ 준금속 원소
- 금속보다는 전기 전도성이 작고, 비금속보다는 전기 전도성이 커서 금속과 비금속의 구분이 명확하지 않은 원소이다.
예) 붕소(B), 규소(Si), 저마늄(Ge), 비소(As) 등
- 규소와 저마늄은 반도체 칩과 태양 전지를 만드는 데 이용된다.
원소의 주기적 성질
(1) 유효 핵전하
① 유효 핵전하:전자에 작용하는 실질적인 핵전하
- 수소 원자는 전자가 1개밖에 없으므로 전자 사이의 반발력은 없고, 원자핵과 전자 사이의 인력만 존재한다. 따라서 수소 원자에서 전자에 작용하는 유효 핵전하는 양성자수에 의한 핵전하와 같은 1+이다.
- 전자가 2개 이상인 다전자 원자에서 전자에 작용하는 실질적인 핵전하를 따지려면 원자핵과 전자 사이의 인력뿐만 아니라 전자 사이의 반발력도 고려해야 한다. 한 전자에 작용하는 유효 핵전하는 다른 전자와의 반발력 때문에 양성자수에 의한 핵전하보다 작아진다.
예) 원자 번호가 6인 탄소(C) 원자의 경우 원자가 전자에 작용하는 유효 핵전하는 양성자수에 의한 핵전하인 6+보다 작다.
② 가려막기 효과(가림 효과)
- 다전자 원자에서 전자에 작용하는 유효 핵전하가 양성자수에 의한 핵전하보다 작아지는 것은 다른 전자에 의해 핵이 가려지기 때문이다. 이러한 현상은 자신보다 안쪽 전자 껍질에 있는 전자뿐만 아니라 자신과 같은 전자 껍질에 있는 다른 전자에 의해서도 나타나며, 이를 가려막기 효과라고 한다.
- 가려막기 효과는 전자 사이의 반발력 때문에 원자핵과 전자 사이의 실질적인 인력이 약해지는 현상을 의미한다.
- 같은 전자 껍질에 있는 전자에 의한 가려막기 효과는 안쪽 전자 껍질에 있는 전자에 의한 가려막기 효과보다 작다.
③ 같은 주기에서 원자 번호에 따른 원자가 전자가 느끼는 유효 핵전하
- 다전자 원자에서 전자에 작용하는 핵전하는 전자 사이의 반발력에 의해 감소하기 때문에
전자에는 양성자수에 의한 핵전하만큼의 인력이 작용하지 못한다.
- 2 주기에서 원자 번호가 1 증가할 때 핵전하(양성자수에 의한 핵전하, 유효 핵전하)의 변화
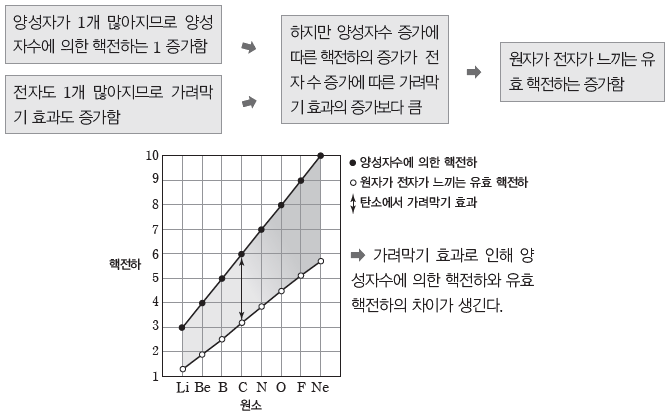
- 2주기에서는 원자 번호가 클수록 원자가 전자가 느끼는 유효 핵전하가 크다.
- 3주기 이상에서도 2주기와 같은 경향을 보인다.
- 18족 원소에서 다음 주기의 1족 원소로 원자 번호가 증가할 때에는 원자가 전자의 껍질이바뀌므로 안쪽 전자 껍질 수가 증가한다. 그러므로 안쪽 껍질의 전자 수 증가로 인한 가려막기 효과가 크게 증가하므로 원자가 전자가 느끼는 유효 핵전하가 감소한다.
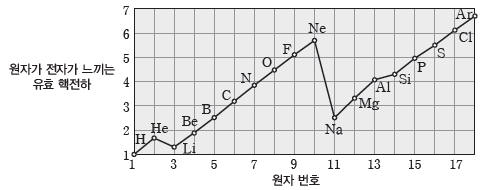
④ 같은 족에서 원자 번호에 따른 원자가 전자가 느끼는 유효 핵전하:같은 족에서 원자 번호가 클수록 원자가 전자가 느끼는 유효 핵전하는 증가한다. 이는 양성자수의 증가에 따른 핵전하의 증가가 전자 수 증가에 따른 가려막기 효과의 증가보다 크기 때문이다.
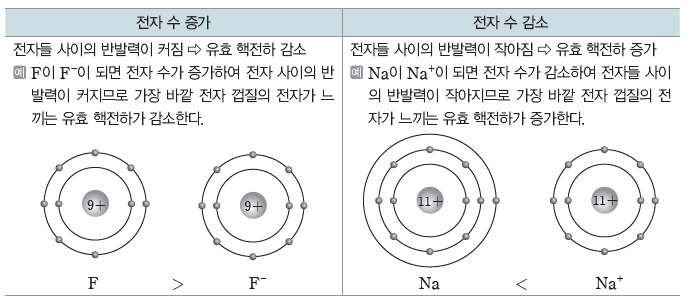
⑤ 전자 수 증가와 감소에 따른 원자가 전자가 느끼는 유효 핵전하
(2) 원자 반지름
① 원자 반지름의 측정
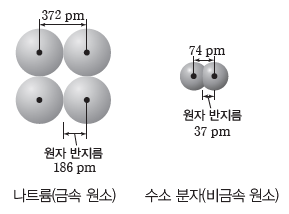
- 현대적 원자 모형인 오비탈 모형에서는 핵으로부터 거리가 아무리 멀어지더라도 전자가 발견될 확률이 0이 되지 않기 때문에 원자의 크기를 정확하게 정의하기 어렵다. 따라서 같은 종류의 두 원자가 결합했을 때 그 두 원자의 원자핵 사이의 거리를 측정하고, 그 거리의 절반을 원자 반지름으로 정의한다.
- 나트륨(Na)과 같은 금속의 경우, 원자 반지름은 나트륨 결정에서 가장 가까운 원자핵 사이 거리의 절반으로 정의한다. 수소(H2), 염소(Cl2)와 같이 동일한 원자로 구성된 이원자 분자의 형태로 존재하는 비금속 원소의 원자 반지름은 원자핵 사이 거리의 절반으로 정의한다.
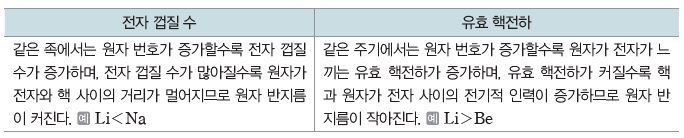
② 원자 반지름에 영향을 주는 요인
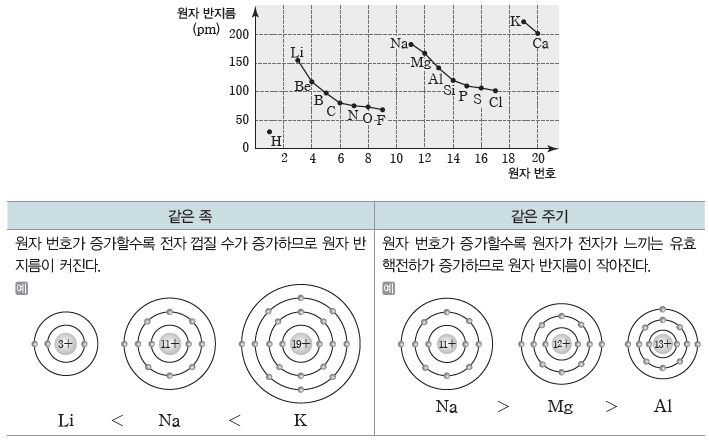
③ 원자 반지름의 주기적 변화(18족 원소 제외)
(3) 이온 반지름
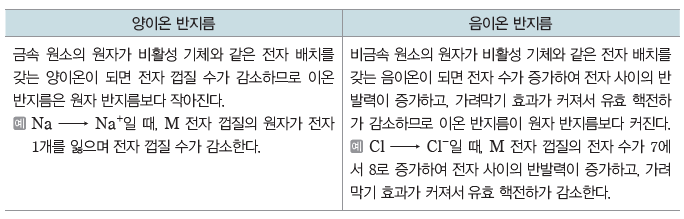
① 이온 반지름의 비교
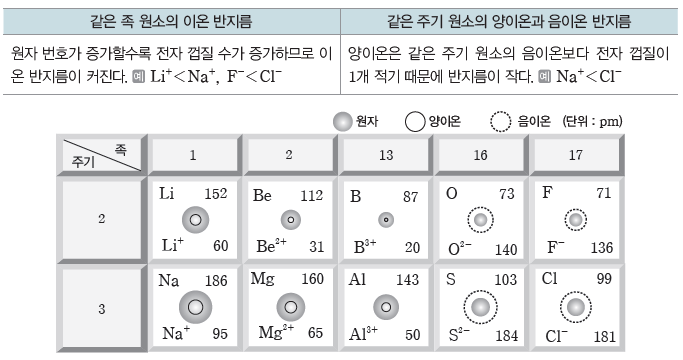
② 전자 수가 같은 이온(등전자 이온)의 이온 반지름
- 전자 수가 같은 이온의 경우 원자 번호가 클수록 유효 핵전하가 크므로 이온 반지름이 작아진다.
- 전자 수가 같은 양이온과 음이온은 원소의 주기가 다르다. 2주기 비금속 원소의 음이온과 3주기 금속 원소의 양이온은 네온(Ne)과 전자 배치가 같은 이온들이고, 3주기 비금속 원소의 음이온과 4주기 금속 원소의 양이온은 아르곤(Ar)과 전자 배치가 같은 이온들이다.

(4) 이온화 에너지:기체 상태의 원자 1 mol에서 전자 1 mol을 떼어 내어 기체 상태의 +1가양이온 1 mol로 만드는 데 필요한 에너지이다.
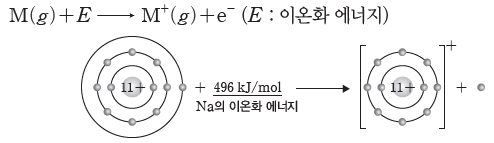
- 이온화 에너지가 작을수록 전자를 떼어 내기가 쉬워지므로 양이온이 되기 쉽다.
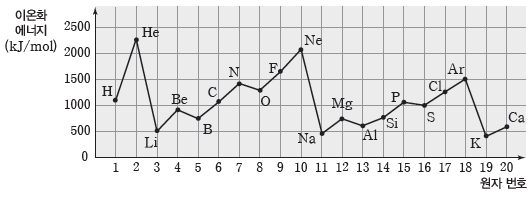
① 이온화 에너지의 주기적 변화

- 2, 3주기에서 2족에서 13족으로 될 때, 15족에서 16족으로 될 때는 이온화 에너지가 감소한다.
- 2주기 원소의 이온화 에너지는 Li<B<Be<C<O<N<F<Ne이다.
- 3주기 원소의 이온화 에너지는 Na<Al<Mg<Si<S<P<Cl<Ar이다.
② 순차 이온화 에너지:기체 상태의 원자 1 mol에서 전자를 1 mol씩 차례대로 떼어 내는 데필요한 단계별 에너지이다.
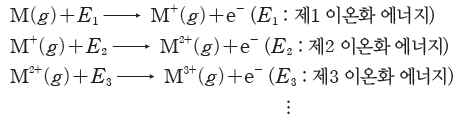
- 전자를 떼어 낼수록 이온의 전자 수가 감소한다. 전자 수가 감소할수록 전자 사이의 반발력이 감소하고 가려막기 효과가 감소하므로 유효 핵전하가 증가하여 다음 전자를 떼어 내기 어려워지므로 순차 이온화 에너지는 차수가 커질수록 증가한다.
⇨ E1<E2<E3<E4<…
- 순차 이온화 에너지 변화와 원자가 전자 수 결정:원자가 전자를 모두 떼어 낸 후, 그 다음전자를 떼어 낼 때는 안쪽 전자 껍질에서 전자가 떨어지게 되어 순차 이온화 에너지가 급격히 증가하게 된다. 따라서 순차 이온화 에너지가 급격히 증가하기 직전까지 떼어 낸 전자 수는 원자가 전자 수와 같다.
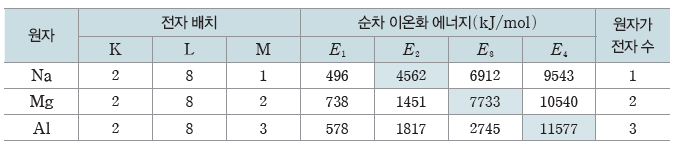
- Na의 경우 순차 이온화 에너지가 E1≪E2<E3이므로 원자가 전자 수가 1이며, Mg의 경우 순차 이온화 에너지가 E1<E2≪E3이므로 원자가 전자 수가 2이다.
- Al의 비활성 기체와 같은 전자 배치를 갖는 이온은 Al3+이며, Al으로부터 Al3+을 생성하기 위한 최소 에너지는 Al의 원자가 전자를 모두 떼어 내는 데 필요한 순차 이온화 에너지의 합(E1+E2+E3)이다.
참고자료: EBS 수능 특강 화학1
