- 원소와 원소의 분류
(1) 원소
① 물질을 이루는 가장 기본적인 성분으로, 더 이상 다른 성분으로 분해되지 않는다.
② 원소의 분류
| 구분 | 금속 | 비금속 |
| 특징 | 전자를 잃고 양이온이 되기 쉬운 원소 | 전자를 얻어 음이온이 되기 쉬운 원소 |
| 성질 | • 실온에서 대부분 고체이다. (단, 수은은 액체)
• 광택이 있다. • 열과 전기 전도성이 있다. • 힘을 가하면 부서지지 않고 모양만 변한다. |
• 실온에서 대부분 고체 또는 기체이다. (단, 브로민은 액체)
• 광택이 없다. • 대부분 열과 전기 전도성이 없다. • 다른 원소와 결합하여 여러 물질을 만든다. |
1-1 다음 설명이 금속에 해당하면 ‘금’, 비금속에 해당하면 ‘비’라고 쓰시오.
⑴ 전자를 잃고 양이온이 되기 쉬운 원소이다. ( )
⑵ 실온에서 대부분 고체 또는 기체 상태로 존재한다. ( )
⑶ 열과 전기 전도성이 있다. ( )
⑷ 외부에서 힘을 가해도 부서지지 않고 모양만 변한다. ( )
1-2 우리 생활에서 이용된 금속 원소와 비금속 원소를 ( ) 안에 쓰시오.
⑴ 각종 철물 및 기계 ( )
⑵ 난방 배관 및 전선 ( )
⑶ 수돗물 소독 ( )
- 주기율표
(1) 현대의 주기율표
① 원소를 원자 번호 순으로 나열하여 화학적 성질이 비슷한 원소들이 같은 세로줄에 오도록 나타낸 표
- 족: 주기율표의 세로줄로, 1~18족까지 존재한다.
- 주기: 주기율표의 가로줄로, 1~7주기까지 존재한다.
② 주기율표에서 금속은 대체로 왼쪽에, 비금속은 대체로 오른쪽에 배치되어 있으며, 왼쪽과 오른쪽 끝에 배치된 원소일수록 반응성이 대체로 크다(18족 원소 제외).
2 현대의 주기율표에 대한 설명 중 옳은 것은 ○, 옳지 않은 것은 ×로 표시하시오.
⑴ 원소를 원자 번호 순서대로 배치하였다. ( )
⑵ 가로줄을 족이라고 하며, 1~18족까지 있다. ( )
⑶ 같은 주기의 원소는 전자가 들어 있는 전자 껍질 수가 같다. ( )
⑷ 같은 주기의 원소들은 원자가 전자 수가 같아 화학적 성질이 비슷하다. ( )
⑸ 1족 원소는 모두 금속 원소이다. ( )
⑹ 2주기에는 모두 8가지 원소가 속해 있다. ( )
- 원자의 전자 배치와 원자가 전자 수
(1) 전자 배치
전자는 원자핵에 가까운 전자 껍질부터 차례로 배치된다.
(2) 원자가 전자
① 가장 바깥 전자 껍질에 있는 전자 중 화학 결합에 참여하는 전자
② 같은 족 원소는 원자가 전자 수가 같으므로 화학적 성질이 비슷하다.
그림은 어떤 원자의 전자 배치 모형을 나타낸 것이다.
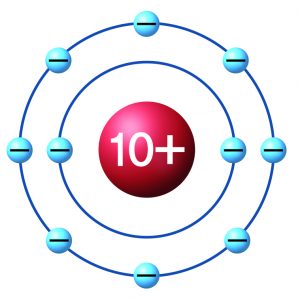
이 원자에 대한 설명 중 옳은 것은 ○, 옳지 않은 것은 ×로 표시하시오.
⑴ 8족 원소이다. ( )
⑵ 2주기 원소이다. ( )
⑶ 원자가 전자 수는 8이다. ( )
- 알칼리 금속과 할로젠 원소
(1) 알칼리 금속
① 수소(H)를 제외한 1족 금속 원소이다.
② 공통적인 성질
- 실온에서 모두 고체이다.
- 다른 금속에 비해 밀도가 작고 무르다.
- 공기 중 산소, 물과 쉽게 반응한다.
(2) 할로젠 원소
① 17족에 속하는 비금속 원소이다.
② 공통적인 성질
- 이원자 분자(F2, Cl2, Br2, I2)로 존재한다.
- 금속과 반응하여 염을 생성한다.
- 수소와 반응하여 수소 화합물을 생성한다.
4-1 다음 설명이 알칼리 금속에 해당하면 ‘알’, 할로젠 원소에 해당하면 ‘할’이라고 쓰시오.
⑴ 원자가 전자 수가 7이다. ( )
⑵ 공기 중에서 쉽게 산소와 반응한다. ( )
⑶ 물과 반응하여 생성된 수용액은 염기성을 띤다. ( )
⑷ 수소 화합물을 물에 녹이면 산성을 띤다. ( )
4-2 다음은 알칼리 금속을 보관하는 방법에 대한 설명이다.
( ) 안에 알맞은 말을 쓰시오.
| 리튬, 나트륨, 칼륨 등의 알칼리 금속은 ( ) 이 커서 공기 중의 ( ), 수증기와 쉽게 반응하므로, 벤젠이나 석유에 넣어 보관한다. |
- 알칼리 금속의 공통적인 성질
알칼리 금속과 물의 반응을 통해 알칼리 금속의 공통적인 성질을 찾아낼 수 있다.
과정
- 유리판에 리튬을 놓고 칼로 잘라 단면을 관찰한다.
- 쌀알 크기의 리튬을 물이 들어 있는 시험관에 넣
고 변화를 관찰한다.
- 2의 시험관에 페놀프탈레인 용액을 2~3방울 넣는다.
- 나트륨과 칼륨을 이용하여 과정 1~3을 반복한다.
결과
| 과정 | 리튬 | 나트륨 | 칼륨 |
| 1 | 서서히 광택을 읽음 | 곧 광택을 잃음 | 자르는 순간 광택을 잃음 |
| 2 | 느리게 기체 발생 | 빠르게 기체 발생 | 격렬하게 기체 발생 |
| 3 | 붉은색 | 붉은색 | 붉은색 |
5 다음 설명 중 옳은 것은 ○, 옳지 않은 것은 ×로 표시하시오.
⑴ 나트륨은 물보다 밀도가 작으므로 물 위에 떠서 반응한다. ( )
⑵ 리튬이 칼륨보다 산소와 더 빠르게 반응한다. ( )
⑶ 칼륨과 물이 반응할 때 발생하는 기체는 수소이다. ( )
⑷ 알칼리 금속이 물과 반응한 후, 수용액에 BTB 용액을 넣으면 노란색으로 변한다. ( )
⑸ 알칼리 금속을 칼로 잘랐을 때 광택을 잃는 까닭은 공기 중 질소와 반응했기 때문이다. ( )
⑹ 알칼리 금속과 물이 반응한 후, 수용액이 페놀프탈레인 용액에 의해 붉게 변한 것은 수용액이 산성을 띠게 되었기 때문이다. ( )
⑺ 리튬, 나트륨, 칼륨이 공통적인 성질을 갖는 까닭은 원자가 전자 수가 같기 때문이다. ( )
자료출처: 지학사 핵심큐 통합과학